آزمایش موتاسیون EGFR | گیرنده فاکتور رشد اپیدرمی | HER-1 | erbB-1
- چرا آزمایش موتاسیون EGFR درخواست می شود؟
- چه زمانی آزمایش موتاسیون EGFR بایستی انجام شود؟
- نمونه مورد نیاز برای آزمایش موتاسیون EGFR :
- روش های مختلف آزمایشگاهی شناسایی موتاسیون EGFR:
- روش واکنش زنجیره ای پلیمراز (PCR):
- واکنش زنجیره ای پلیمراز (PCR) | Polymerase Chain Reaction
- روش توالی یابی سانگر:
- روش توالی نسل بعدی (NGS):
- NGS | توالی یابی نسل بعدی | Next-generation sequencing | توالی یابی با توان بالا | High-throughput sequencing
- روش سیستم جهش مقاوم در برابر تقویت (ARMS):
- روش هیبریداسیون درجا فلورسانس (FISH):
- روش بیوپسی مایع:
- آزمایش بیوپسی مایع | DNA تومور در گردش (ctDNA) | Liquid biopsy | سلول های تومور در گردش (CTC) | Circulating Tumor Cell Count
- آمادگی قبل از انجام آزمایش موتاسیون EGFR:
- چه چیزی در آزمایش موتاسیون EGFR مورد بررسی قرار می گیرد؟
- ملاحظات بالینی:
- سوالات متداول
- چگونه از نتایج آزمایش موتاسیون EGFR استفاده می شود؟
- چه زمانی آزمایش موتاسیون EGFR درخواست می شود؟
- نتیجه آزمایش موتاسیون EGFR چه چیزی را نشان می دهد؟
- آیا چیز دیگری هست که باید بدانم؟
- چه آزمایش دیگری ممکن است در کنار آزمایش موتاسیون EGFR درخواست شود؟
- آماده شدن نتایج آزمایش موتاسیون EGFR چقدر طول می کشد؟
- آیا می توان به جای بیوپسی بافتی از آزمایش خون برای موتاسیون EGFR استفاده کرد؟
- تفاوت بین EGFR (همچنین به عنوان HER-1 شناخته می شود) و HER-2 چیست؟
- آزمایش HER2 | گیرنده ۲ فاکتور رشد اپیدرمی انسانی | HER2/neu | HercepTest | c-erbB-2
- آیا آزمایش های دیگری وجود دارد که EGFR را در تومورها ارزیابی کند؟
- به جز سرطان ریه، در چه سرطان های دیگری مقدار پروتئین EGFR افزایش می یابد؟
- مطالب مرتبط در متااورگانون:
- تومور مارکر | Tumor Markers
- بازآرایی (ژن ALK) | ALK (گیرنده لنفوم آناپلاستیک تیروزین کیناز) | EML4-ALK Fusion Protein
- آزمایش های ژنتیکی برای درمان هدفمند سرطان
- آزمایش جهش KRAS
- آزمایش بیوپسی مایع | DNA تومور در گردش (ctDNA) | Liquid biopsy | سلول های تومور در گردش (CTC) | Circulating Tumor Cell Count
- در جای دیگر وب:
آزمایش موتاسیون EGFR جهش در ژن EGFR را بررسی می کند . EGFR (گیرنده فاکتور رشد اپیدرمی) پروتئینی روی سلول ها است که به رشد آنها کمک می کند. جهش در ژن EGFR می تواند باعث رشد و تقسم بیش از حد سلول ها شود که در نهایت می تواند باعث سرطانی شدن آن سلول ها شود. انواع مختلفی از جهش های EGFR وجود دارد.
اسامی دیگر:
- HER-1
- erbB-1
- Epidermal Growth Factor Receptor Mutation Analysis
- Epidermal Growth Factor Receptor
چرا آزمایش موتاسیون EGFR درخواست می شود؟
آزمایش جهش EGFR (گیرنده فاکتور رشد اپیدرمی) برای چندین هدف مهم در زمینه انکولوژی و پزشکی شخصی درخواست شده است. در اینجا دلیل انجام این آزمون و اهداف اصلی آن آمده است:
- انتخاب درمان: جهش های گیرنده فاکتور رشد اپیدرمی معمولا در سرطان ریه سلول غیر کوچک (NSCLC) یافت می شود. شناسایی این جهش ها به انکولوژیست ها کمک می کند تا مناسب ترین درمان هدفمند را برای بیمار تعیین کنند. داروهایی مانند جفیتینیب، ارلوتینیب و اوزیمرتینیب به طور خاص سلول های سرطانی را با جهش های EGFR هدف قرار می دهند که منجر به نتایج درمانی موثرتری می شود.
- اطلاعات پیش آگهی: وضعیت جهش گیرنده فاکتور رشد اپیدرمی می تواند اطلاعات پیش آگهی ارزشمندی را ارائه دهد. بیماران مبتلا به جهشهای خاص EGFR ممکن است پاسخ بهتری به درمانهای هدفمند داشته باشند و بنابراین، پیشآگهی بالقوه بهتری در مقایسه با بیماران بدون این جهشها دارند.
- پزشکی شخصی: آزمایش جهش گیرنده فاکتور رشد اپیدرمی نمونه بارز پزشکی شخصی است. با تنظیم درمان بر اساس مشخصات ژنتیکی خاص بیمار، ارائه دهندگان مراقبت های بهداشتی به طور بالقوه می توانند عوارض جانبی را به حداقل برسانند و کارایی درمان را بهبود بخشند.
- نظارت بر اثربخشی درمان: آزمایش جهش گیرنده فاکتور رشد اپیدرمی سریال ممکن است در طول دوره درمان برای نظارت بر نحوه پاسخ سرطان انجام شود. تغییرات در وضعیت جهش EGFR می تواند تنظیمات درمان را هدایت کند.
- تحقیق و کارآزمایی های بالینی: آزمایش جهش گیرنده فاکتور رشد اپیدرمی برای ثبت نام بیمار در کارآزمایی های بالینی که درمان های هدفمند جدید را بررسی می کنند، بسیار مهم است. این به محققان کمک می کند تا نامزدهای مناسب برای درمان های تجربی را شناسایی کنند و به پیشرفت تحقیقات سرطان کمک می کند.
- تصمیمات هدایت کننده جراحی: در برخی موارد، وضعیت جهش گیرنده فاکتور رشد اپیدرمی می تواند بر تصمیمات مربوط به برداشتن جراحی تومورهای ریه تأثیر بگذارد. بیماران مبتلا به جهش های خاص EGFR ممکن است از جراحی در ترکیب با درمان های هدفمند بهره بیشتری ببرند.
- پیش بینی مقاومت: در حالی که درمان های هدفمند گیرنده فاکتور رشد اپیدرمی می توانند در ابتدا موثر باشند، مقاومت می تواند در طول زمان ایجاد شود. آزمایش مداوم جهش EGFR میتواند به پیشبینی ظهور جهشهای مقاومتی کمک کند و امکان تنظیم به موقع درمان را فراهم کند.
توجه به این نکته مهم است که دلایل خاص برای آزمایش جهش گیرنده فاکتور رشد اپیدرمی ممکن است بسته به زمینه بالینی و نوع سرطان مورد ارزیابی متفاوت باشد. علاوه بر این، رشته سرطان شناسی به طور مداوم در حال پیشرفت است، بنابراین به روز ماندن با آخرین دستورالعمل های تحقیقاتی و درمانی برای متخصصان آزمایشگاه پزشکی مانند شما بسیار مهم است.
چه زمانی آزمایش موتاسیون EGFR بایستی انجام شود؟
- زمانی که سرطان ریه سلول غیر کوچک تشخیص داده شد.
- هنگام در نظر گرفتن استفاده از درمان های هدفمند EGFR، مانند جفیتینیب، ارلوتینیب، یا اوزیمرتینیب، آزمایش جهش EGFR ضروری است. این داروها در بیماران مبتلا به جهش های خاص EGFR مانند حذف اگزون 19 یا جهش L858R بیشترین تاثیر را دارند.
- اگر NSCLC بیمار پس از درمان اولیه پیشرفت کند، ممکن است آزمایش جهش EGFR در نظر گرفته شود. شناسایی جهشهای جدید، از جمله جهش EGFR T790M، میتواند به راهنمایی گزینههای درمانی بعدی کمک کند.
- زمانی که تحت درمان با مهارکننده تیروزین کیناز هدفمند EGFR هستید، اما سرطان همچنان در حال پیشرفت است و به درمان پاسخ نمی دهد.
نمونه مورد نیاز برای آزمایش موتاسیون EGFR :
- ظرف/لوله: بلوک یا اسلایدهای بافتی ثابت با فرمالین، جاسازی شده در پارافین (FFPE) از NSCLC
- نوع نمونه: بافت سرطانی
- حجم نمونه: پنج اسلاید رنگآمیزی و یک لام رنگآمیزی شده با هماتوکسیلین ائوزین یا بلوک بافتی ثابت شده با فرمالین و پارافین
گاها نمونه خون گرفته شده از ورید (بیوپسی مایع) لوله با دربب بنفش حاوی ضد انعقاد EDTA ممکن است در برخی شرایط استفاده شود.
گزارش پاتولوژی باید همراه نمونه باشد تا آزمایش انجام شود.

بلوک تومور حاوی تومور ناکافی؛ بافت یا تومور ثابت شده در فیکساتور فلزات سنگین؛ اسلایدهای شکسته یا لکه دار
شاید این مطلب برای شما مفید باشد:
روش های مختلف جمع آوری نمونه های آزمایشگاه
شاید این مطلب برای شما مفید باشد:
لوله های آزمایش و ضد انعقادها (Test tubes and Anticoagulants)
شاید این مطلب برای شما مفید باشد:
ذخیره سازی نمونه های آزمایشگاهی
روش های مختلف آزمایشگاهی شناسایی موتاسیون EGFR:
شناسایی جهشهای EGFR (گیرنده فاکتور رشد اپیدرمی) در تشخیص و درمان برخی سرطانها، بهویژه سرطان ریه سلولهای غیر کوچک (NSCLC) ضروری است. روش های مختلفی در آزمایشگاه های بالینی برای شناسایی این جهش ها استفاده می شود.
روش واکنش زنجیره ای پلیمراز (PCR):
- اصل: PCR تکنیکی است که برای تکثیر توالی های خاص DNA استفاده می شود. در آزمایش جهش EGFR، PCR نواحی خاصی از ژن EGFR را هدف قرار می دهد که در آن جهش ها مشخص است.
- Real-Time PCR: در این روش از کاوشگرهای فلورسنت استفاده می شود که همزمان با تقویت DNA سیگنالی را منتشر می کنند. این امکان را برای نظارت در زمان واقعی تقویت و تشخیص جهش فراهم می کند. Real-time PCR سریع است و اغلب برای جهش های رایج EGFR، مانند جهش L858R و حذف اگزون 19 استفاده می شود.
شاید این مطلب برای شما مفید باشد:
واکنش زنجیره ای پلیمراز (PCR) | Polymerase Chain Reaction
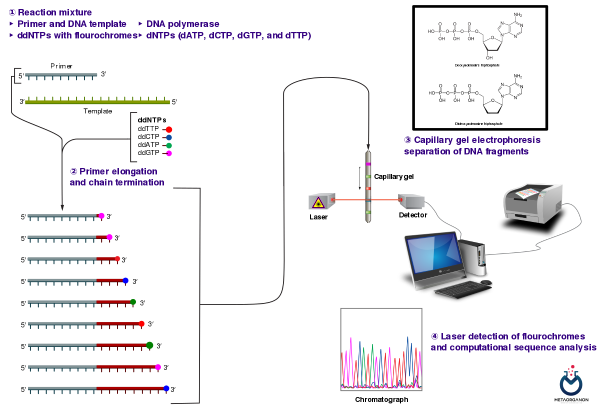
روش توالی یابی سانگر:
- اصل: توالی یابی سانگر یک روش سنتی توالی یابی DNA است که ترتیب نوکلئوتیدها را در یک رشته DNA تعیین می کند.
- روش: DNA از نمونه بیمار توالی یابی می شود. توالی با یک توالی EGFR مرجع برای شناسایی جهش مقایسه می شود.
- استفاده: توالی سنجی Sanger می تواند طیف وسیعی از جهش های EGFR را تشخیص دهد اما ممکن است در تشخیص جهش های فرکانس پایین محدودیت هایی داشته باشد.
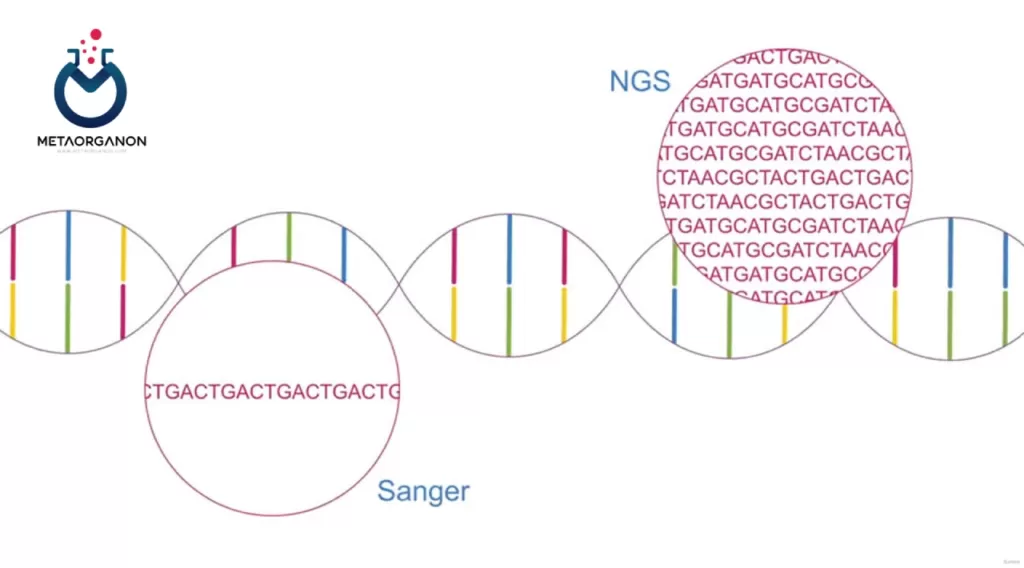
روش توالی نسل بعدی (NGS):
- اصل: NGS یک تکنیک توالی یابی با توان عملیاتی بالا است که می تواند چندین ژن از جمله گیرنده فاکتور رشد اپیدرمی را به طور همزمان تجزیه و تحلیل کند.
- هدف: این رویکرد از پانل هایی استفاده می کند که برای هدف قرار دادن مناطق ژنومی خاص، از جمله EGFR طراحی شده اند. کارآمد است و می تواند طیف وسیعی از جهش ها را تشخیص دهد.
- استفاده: توالی یابی کل اگزوم یا توالی یابی کل ژنوم می تواند جهش های EGFR را شناسایی کند اما بیشتر پژوهش محور است و معمولاً برای آزمایش های بالینی معمول استفاده نمی شود.
شاید این مطلب برای شما مفید باشد:
NGS | توالی یابی نسل بعدی | Next-generation sequencing | توالی یابی با توان بالا | High-throughput sequencing
روش سیستم جهش مقاوم در برابر تقویت (ARMS):
- اصل: ARMS-PCR یک تکنیک بسیار خاص مبتنی بر PCR است که برای تشخیص جهش های خاص، از جمله جهش های گیرنده فاکتور رشد اپیدرمی طراحی شده است.
- روش: PCR با استفاده از پرایمرهایی انجام می شود که به طور خاص جهش مورد نظر را تشخیص می دهند. اگر جهش وجود داشته باشد، تقویت رخ می دهد.
- استفاده: ARMS-PCR به دلیل حساسیت بالا در شناسایی جهش ها شناخته شده است و برای تشخیص جهش های خاص گیرنده فاکتور رشد اپیدرمی مناسب است.
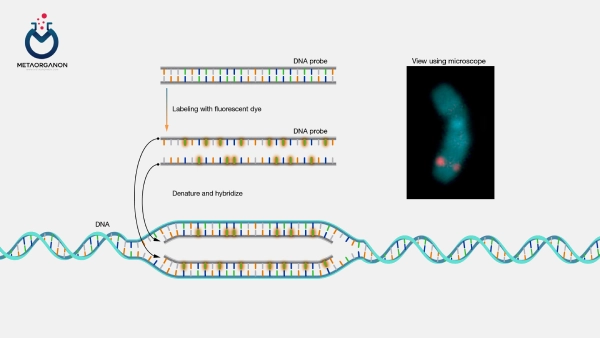
روش هیبریداسیون درجا فلورسانس (FISH):
- اصل: FISH یک تکنیک سیتوژنتیک است که از پروب های فلورسنت برای شناسایی تغییرات ژنی، از جمله تقویت ژن EGFR استفاده می کند.
- روش: پروب های DNA مخصوص ژن EGFR روی نمونه های بیمار اعمال می شود. وجود کپی های اضافی EGFR (تقویت) در زیر میکروسکوپ فلورسانس تشخیص داده می شود.
- استفاده: FISH برای شناسایی بیمارانی استفاده می شود که ممکن است به درمان های هدفمند EGFR بر اساس تقویت ژن EGFR پاسخ دهند.
روش بیوپسی مایع:
- اصل: بیوپسی های مایع DNA بدون سلول (cfDNA) یا DNA تومور در گردش (ctDNA) را در نمونه های خون برای تشخیص جهش تجزیه و تحلیل می کنند.
- روش: تکنیک هایی مانند PCR دیجیتال یا NGS را می توان در نمونه های بیوپسی مایع اعمال کرد.
- استفاده: بیوپسی های مایع برای نظارت بر پیشرفت بیماری و پاسخ درمانی ارزشمند هستند و می توانند برای تشخیص جهش های EGFR در مواردی که بیوپسی بافتی چالش برانگیز است استفاده شود.
شاید این مطلب برای شما مفید باشد:
آزمایش بیوپسی مایع | DNA تومور در گردش (ctDNA) | Liquid biopsy | سلول های تومور در گردش (CTC) | Circulating Tumor Cell Count
انتخاب روش به عواملی مانند جهشهای خاص گیرنده فاکتور رشد اپیدرمی، زمینه بالینی، تجهیزات موجود و اهداف آزمایش بستگی دارد. در عمل بالینی، ترکیبی از روش ها ممکن است برای اطمینان از تجزیه و تحلیل دقیق و جامع جهش EGFR استفاده شود.
آمادگی قبل از انجام آزمایش موتاسیون EGFR:
در بسیاری از موارد آمادگی لازم نیست، اما بستگی به نحوه به دست آوردن سلول های سرطانی دارد. بر اساس روشی که برای به دست آوردن نمونه استفاده می شود، دستورالعمل هایی از پزشک خود دریافت خواهید کرد.
چه چیزی در آزمایش موتاسیون EGFR مورد بررسی قرار می گیرد؟
سرطان ریه یکی از عوامل اصلی مرگ و میر ناشی از سرطان در جهان است. سرطان ریه سلول غیر کوچک (NSCLC) 70 تا 85 درصد از همه تشخیصهای سرطان ریه را تشکیل میدهد. عوامل دارویی مولکولی کوچکی که دامین تیروزین کیناز پروتئین گیرنده فاکتور رشد اپیدرمی (EGFR) را هدف قرار می دهند، برای درمان NSCLC در موارد موضعی پیشرفته یا متاستاتیک به عنوان یک رژیم خط دوم یا سوم تایید شده اند.
کارآزماییهای مختلف نشان دادهاند که عوامل هدف به تنهایی یا همراه با شیمیدرمانی ممکن است در مراقبتها و تنظیمات خط اول مفید باشند. از آنجایی که شیمی درمانی منجر به افزایش سمیت، و عوارض زیاد و همچنین هزینه های جانبی می شود، راه کارهایی که به شناسایی افرادی که احتمالاً از درمان های هدفمند سود می برند میتواند بسیار کمک کننده باشد.
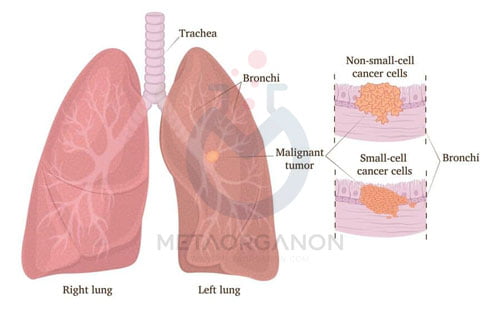
سرطانهای سلول غیر کوچک ریه (NSCLC)
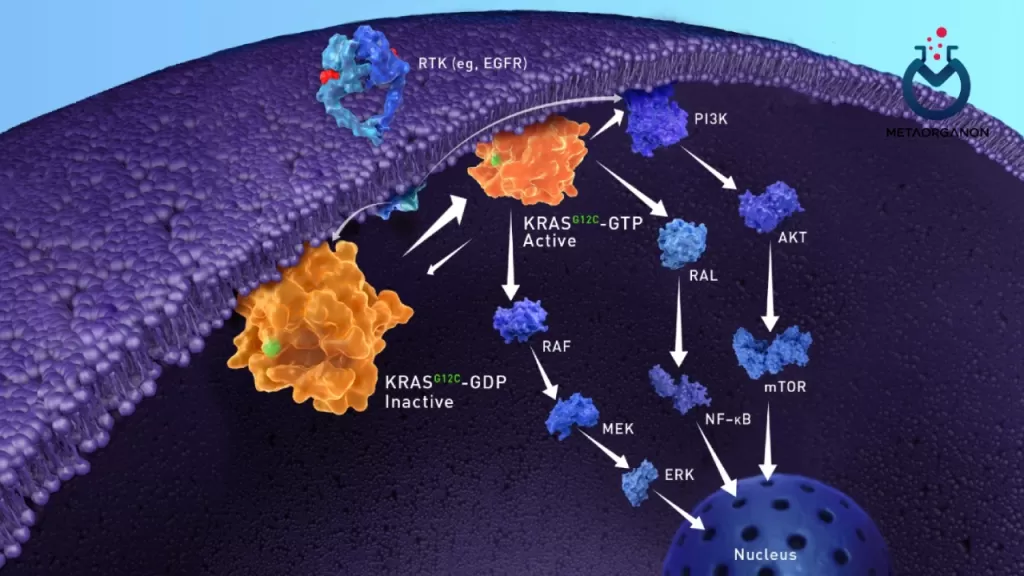
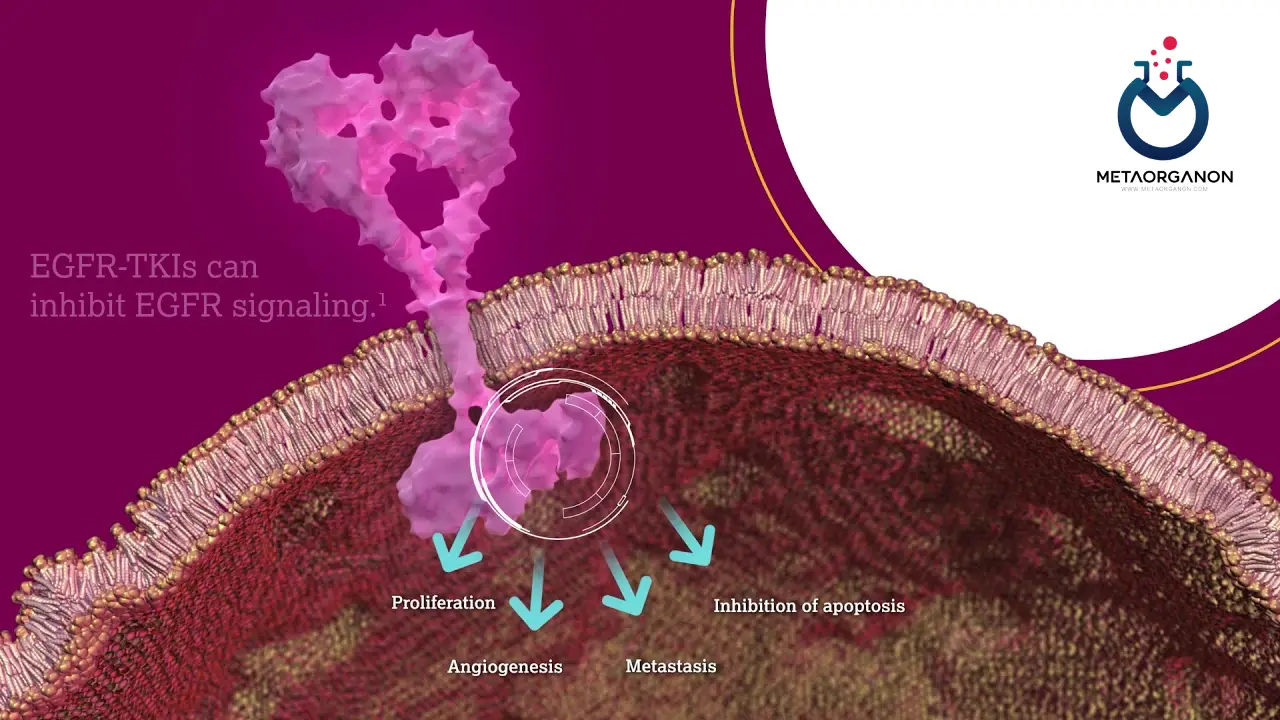
EGFR یک گیرنده فاکتور رشد است که با اتصال لیگاندهای خاص فعال می شود و در نتیجه مسیر RAS/MAPK فعال می شود. فعال شدن این مسیر باعث ایجاد یک آبشار سیگنالینگ می شود که در نهایت منجر به تکثیر سلولی می شود. اختلال در مسیر RAS/MAPK یک عامل کلیدی در پیشرفت تومور برای بسیاری از تومورهای جامد است. درمانهای هدفمند برای تومورهایی که دارای جهشهای فعال کننده در دامین تیروزین کیناز EGFR (اگزونهای 18 و 21) هستند، موفقیتهایی را در درمان زیرمجموعهای از بیماران مبتلا به NSCLC با جلوگیری از اتصال آدنوزین ‘5-تری فسفات (ATP) در جایگاه فعال نشان دادهاند.
Gefitinib و Erlotinib توسط FDA برای استفاده در درمان بیماران مبتلا به NSCLC که قبلاً به شیمیدرمانی مبتنی بر پلاتین سنتی پاسخ نمیدادند تأیید شدهاند. همچنین اخیراً نشان داده شده است که این دو دارو طول عمر را بدون پیشرفت سرطان را در بیمارانی که درمان با مهارکننده EGFR-تیروزین کیناز را به عنوان درمان خط اول برای درمان NSCLC دریافت میکنند، افزایش میدهند.
عواملی مانند Gefitinib و Erlotinib که از اتصال ATP به EGFR کیناز جلوگیری می کنند، به نظر می رسد که فعالیت مهارکننده معنی داری روی تومورهایی که جهش T790M EGFR خاص مقاوم به دارو را نشان می دهند، داشته باشند. بنابراین، دادههای کنونی نشان میدهد که اثربخشی درمانهای هدفمند EGFR در NSCLC محدود به بیماران مبتلا به تومورهایی است که دارای جهشهای فعالکننده EGFR مانند L858R، L861Q، G719A/S/C، S768I یا حذفهای کوچک در اگزون 19 و عدم وجود جهش T790M مقاوم به دارو باشند. در نتیجه، وضعیت جهش EGFR می تواند نشانگر مفیدی در انتخاب درمان برای بیماران مبتلا به NSCLC باشد.
ملاحظات بالینی:
آزمایش موتاسیون گیرنده فاکتور رشد اپیدرمی برای تشخیص جهش در اگزون های 18، 19، 20 و 21 ژن EGFR طراحی شده است. این جهش ها بیش از 99 درصد از تمام جهش های گزارش شده EGFR در بیماران NSCLC را تشکیل می دهند. نمونه هایی با نتایج گزارش شده به عنوان “هیچ جهشی شناسایی نشده” ممکن است دارای موتاسیون EGFR باشند که توسط آزمایش تشخیص داده نمی شوند.
تشخیص جهش به یکپارچگی نمونه و مقدار DNA استخراج شده موجود در نمونه بستگی دارد. روشهای مورد استفاده در این آزمایش بسیار انتخابی هستند و بسته به مقدار کل DNA موجود، میتوانند تقریباً 2 تا 20 درصد ژن جهش یافته را در DNA ژنومی شناسایی کنند.
سوالات متداول
چگونه از نتایج آزمایش موتاسیون EGFR استفاده می شود؟
وجود جهش در ژن گیرنده فاکتور رشد اپیدرمی را در DNA سلولهای تومور تشخیص میدهد تا به تعیین اینکه آیا فرد مبتلا به سرطان ریه سلول غیرکوچک (NSCLC) ممکن است از درمان هدفمند با مهارکنندههای تیروزین کیناز (TKIs) مانند Gefitinib و Erlotinib استفاده کند یا خیر. موتاسیون های خاص EGFR می تواند منجر به رشد کنترل نشده سلول های سرطانی شود. TKI ها می توانند از عملکرد EGFR برای مهار رشد سلول های سرطانی جلوگیری کنند.
آزمایش موتاسیون گیرنده فاکتور رشد اپیدرمی ممکن است به تنهایی یا به عنوان بخشی از یک پانل (یک سری آزمایش برای تشخیص جهش در ژنهای دیگر مانند KRAS، ALK و ROS1) درخواست شود. هر یک از این آزمایشها ممکن است برای کمک به تعیین اینکه آیا سرطان ریه فرد به درمان هدفمند پاسخ میدهد و اینکه کدام نوع سودمندتر است، استفاده شود.

داروهای درمانی موتاسیون EGFR
علاوه بر این، ممکن است پس از شروع درمان از آزمایش برای تعیین اینکه آیا سرطان جهشهای جدیدی کسب کرده است که آن را به درمان فعلی مقاوم میکند، استفاده شود. برای مثال، یکی از جهشهای مقاومت شناختهشده، بهویژه T790M، ممکن است شناسایی شود و سپس میتوان آن را با داروی دیگری که مخصوصاً برای این جهش خاص طراحی شده است، هدف قرار داد.
چه زمانی آزمایش موتاسیون EGFR درخواست می شود؟
آزمایش موتاسیون گیرنده فاکتور رشد اپیدرمی پس از تشخیص سرطان ریه سلول غیر کوچک، به ویژه آدنوکارسینوما، درخواست می شود.
هنگامی که یک بیمار قبلاً با مهارکننده تیروزین کیناز هدفمند EGFR درمان شده است، اما به نظر نمی رسد که به درمان پاسخ مثبتی بدهد، پزشک ممکن است آزمایش موتاسیون EGFR را بر روی یک نمونه جدید برای بررسی موتاسیون های خاص EGFR درخواست کند. به دلیل عدم پاسخ مطلوب یک نمونه جدید از بافت تومور، یا گاهی اوقات یک نمونه خون، برای تعیین اینکه آیا سرطان جهشهای جدیدی کسب کرده است که آن را در برابر درمان فعلی مقاوم میکند، مورد نیاز است.
نتیجه آزمایش موتاسیون EGFR چه چیزی را نشان می دهد؟
اگر سرطان ریه فردی دارای یک موتاسیون حساس کننده EGFR باشد، ممکن است یک مهارکننده تیروزین کیناز (TKI) هدفمند EGFR در درمان تومور موثر باشد. اگر هیچ جهش حساس کننده ای با آزمایش EGFR تشخیص داده نشود، احتمال کمتری دارد که تومور به درمان TKI پاسخ دهد. گاهی اوقات یک جهش EGFR تشخیص داده می شود، اما نشان می دهد که سرطان به TKI پاسخ نمی دهد.پاتولوژیست ها و متخصصان سرطان (انکولوژیست ها) به تفسیر اهمیت دقیق موتاسیون EGFR شناسایی شده برای هر بیمار کمک می کنند.
آیا چیز دیگری هست که باید بدانم؟
آزمایش موتاسیون گیرنده فاکتور رشد اپیدرمی معمولاً برای شناسایی موتاسیون های گیرنده فاکتور رشد اپیدرمی که با اهمیت و شایع هستند بهینه می شود، اما ممکن است جهش های گیرنده فاکتور رشد اپیدرمی غیر معمول یا منحصر به فردی در تومور وجود داشته باشد که شناسایی نشده باشد.
اگرچه ممکن است یک جهش در سلول های تومور وجود داشته باشد، اما اگر بافت تومور بسیار کمی وجود داشته باشد و/یا زمانی که سلول های توموری حاوی جهش، به مقدار کافی وجود نداشته باشد، آزمایش ممکن است علیرغم وجود جهش در سلول های تومور منجر به نتیجه “هیچ جهشی شناسایی نشده” شود.
از آنجایی که مقدار DNA تومور در نمونه خون نامشخص است، آزمایش نمونه خون (که بیوپسی مایع نیز نامیده می شود) معمولاً ترجیح داده نمی شود. با این حال، در شرایطی که سلولهای تومور کافی برای آزمایش مولکولی از بیوپسی بافتی در دسترس نباشند، یا در شرایطی که نمونهبرداری بافتی قابل انجام نیست، آزمایش خون (بیوپسی مایع) ممکن است یک روش آزمایش جایگزین قابل قبول باشد.
موتاسیون های شناخته شده حساس کننده EGFR معمولاً منجر به تغییرات در مناطق کوچک پروتئین EGFR می شود. آزمایش این نوع جهشها معمولاً با تکنیکهایی مانند Real time PCR یا next generation sequencing انجام میشود.
چه آزمایش دیگری ممکن است در کنار آزمایش موتاسیون EGFR درخواست شود؟
آزمایش جهش ALK و/یا ROS1 برای تعیین اینکه آیا تومور فرد احتمالاً به درمانهای هدفمند خاصی پاسخ میدهد گاها توصیه میشود. در صورتی که نمونه بافتی کافی در دسترس باشد، ممکن است برای بیماران سرطان ریه آزمایش برای جهش در ژنهای دیگر (به عنوان مثال، KRAS) درخواست شود.
آماده شدن نتایج آزمایش موتاسیون EGFR چقدر طول می کشد؟
آزمایش موتاسیون گیرنده فاکتور رشد اپیدرمی در هر آزمایشگاهی در دسترس نیست. اگر پزشک نمونه را به آزمایشگاه مرجع بفرستد، بسته به روش آزمایشی مورد استفاده، نتایج ممکن است چند روز الی چند هفته طول بکشد تا آماده شود.
آیا می توان به جای بیوپسی بافتی از آزمایش خون برای موتاسیون EGFR استفاده کرد؟
برای تشخیص تومور، به بیوپسی بافت نیاز دارید. علاوه بر این، آزمایش خون برای DNA تومور در گردش (ctDNA) که بیوپسی مایع نیز نامیده میشود، ممکن است برای شناسایی جهشهای EGFR در تومور انجام شود که میتواند پاسخدهی بالقوه یا مقاومت به درمانهای هدفمند را پیشبینی کند.
آزمایش CtDNA ممکن است برای شناسایی جهش هایی که تومور را به درمان هدفمند حساس می کنند (جهش های حساس کننده) استفاده شود. با این حال، آزمایش ctDNA گاهی اوقات نتایج منفی کاذب می دهد (به این معنی که جهش وجود دارد اما با آزمایش ctDNA تشخیص داده نمی شود). به همین دلیل، FDA بیوپسی بافت را در صورتی که بیوپسی مایع منفی باشد (جهش حساس کننده را تشخیص نمی دهد) توصیه می کند.
علاوه بر این، بیوپسی مایع ممکن است برای تشخیص جهش EGFR T790M استفاده شود که باعث مقاومت در برابر درمان هدفمند می شود. با این حال، در حال حاضر داده ها در این مورد محدود است، بنابراین بیوپسی مایع تنها در صورتی می تواند مورد استفاده قرار گیرد که نمونه برداری بافتی به دست نیاید.
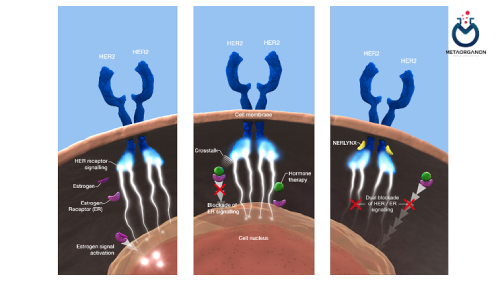
تفاوت بین EGFR (همچنین به عنوان HER-1 شناخته می شود) و HER-2 چیست؟
EGFR و HER-2 هر دو عضو یک خانواده از گیرنده های غشای سلولی هستند. هنگامی که EGFR یا HER-2 به طور قابل توجهی در سرطان افزایش می یابد، اغلب نشان دهنده تومور تهاجمی تر و پیش آگهی ضعیف تر بیمار به درمان است. تفاوت اصلی بین آزمایش EGFR و HER-2 این است که از آنها برای کمک به ارزیابی انواع مختلف سرطان درخواست می شوند و داروهایی که براساس نتایج آزمایش برای هدف قرار دادن آنها ساخته می شوند برای گیرنده های EGFR یا HER-2،اختصاصی هستند. HER-2 در سرطان سینه و سرطان معده و مری (آدنوکارسینوم معده مری) ارزیابی می شود.
شاید این مطلب برای شما مفید باشد:
آزمایش HER2 | گیرنده ۲ فاکتور رشد اپیدرمی انسانی | HER2/neu | HercepTest | c-erbB-2
آیا آزمایش های دیگری وجود دارد که EGFR را در تومورها ارزیابی کند؟
آزمایشهایی وجود دارد که تغییرات دیگری را در گیرنده فاکتور رشد اپیدرمی به نام تقویت ژن شناسایی میکند، به این معنی که مقدار کمی(تعداد) نسخههای غیرطبیعی ژن EGFR را که در سلولهای تومور وجود دارد شناسائی می کند.
نوع دیگری از آزمایش میزان پروتئین گیرنده فاکتور رشد اپیدرمی موجود در سلول های تومور را بررسی می کند. این آزمایش ها برای شناسایی بیماران مبتلا به سرطان ریه که ممکن است از درمان با مهارکننده تیروزین کیناز هدفمند گیرنده فاکتور رشد اپیدرمی سود ببرند، مفید نیستند. با این حال، ممکن است در انواع دیگر سرطان نقش داشته باشند. به عنوان مثال، گاهی از آزمایشهای تقویت ژن EGFR برای تعیین سیر احتمالی (پیشآگهی) سرطان سر و گردن استفاده میشود.
به جز سرطان ریه، در چه سرطان های دیگری مقدار پروتئین EGFR افزایش می یابد؟
سرطان های دیگری که ممکن است پروتئین گیرنده فاکتور رشد اپیدرمی را افزایش دهند عبارتند از سرطان روده بزرگ، گلیوبلاستوما (نوعی سرطان مغز)، سرطان های سر و گردن، سینه و پانکراس. داروهای مسدود کننده EGFR به طور معمول برای درمان سرطان متاستاتیک کولون استفاده می شود و برای برخی از سرطان های سر و گردن استفاده می شود. کاربرد مهارکنندههای EGFR و ارتباط آنها با جهشهای EGFR در انواع مختلف سرطان به طور کامل ثابت نشده است، اما همچنان مورد بررسی قرار میگیرد.
در سایت WebMD در مورد موتاسیون EGFR بیشتر بخوانید:
گیرنده فاکتور رشد اپیدرمی (EGFR) پروتئینی روی سطح سلول های شما است که به رشد آنها کمک می کند. زمانی که ژن کد کننده EGFR دارای جهش باشد، بر نحوه عملکرد این پروتئین تأثیر می گذارد و باعث سرطان می شود. انواع مختلفی از جهش های EGFR وجود دارد.
مطالب مرتبط در متااورگانون:
شاید این مطلب برای شما مفید باشد:
تومور مارکر | Tumor Markers
شاید این مطلب برای شما مفید باشد:
بازآرایی (ژن ALK) | ALK (گیرنده لنفوم آناپلاستیک تیروزین کیناز) | EML4-ALK Fusion Protein
شاید این مطلب برای شما مفید باشد:
آزمایش های ژنتیکی برای درمان هدفمند سرطان
شاید این مطلب برای شما مفید باشد:
آزمایش جهش KRAS
شاید این مطلب برای شما مفید باشد:
آزمایش بیوپسی مایع | DNA تومور در گردش (ctDNA) | Liquid biopsy | سلول های تومور در گردش (CTC) | Circulating Tumor Cell Count
در جای دیگر وب:
- Genetics Home Reference: How Genes Work
- American Cancer Society: Targeted Cancer Therapy
- American Cancer Society: Targeted Therapy Drugs for Non-Small Cell Lung Cancer
- National Cancer Institute: Lung Cancer
- National Cancer Institute, Targeted Cancer Therapies
- MedlinePlus Medical Encyclopedia: Lung cancer – non-small cell
منابع مقاله
Yatabe Y. Updated Molecular Testing Guideline for the Selection of Lung Cancer Patients for Treatment With Targeted Tyrosine Kinase Inhibitors: Guideline From the College of American Pathologists, the International Association for the Study of Lung Cancer, and the Association for Molecular Pathology. Arch Pathol Lab Med. 2018 Jan 22. Available online at http://www.archivesofpathology.org/doi/pdf/10.5858/arpa.2017-0388-CP
Mishra R, Hanker AB, Garrett JT. Genomic alterations of ERBB receptors in cancer: clinical implications. Oncotarget. 2017 Nov 30;8(69):114371-114392
(August 27, 2007) NCCN Guidelines Version 2.2018 Panel Members. Non-Small Cell Lung Cancer. NCCN Clinical Practice Guidelines in Oncology. Available online at https://www.nccn.org/professionals/physician_gls/default.aspx. Accessed on 1/31/2018
(© 2018). EGFR T790M Mutation in Circulating Tumor DNA by Digital Droplet PCR. ARUP Laboratories. Available online at https://www.aruplab.com/T790M. Accessed June 2019
Bronner, M. Revolutionizing Treatment for Cancer Care: New Circulating Cell-Free Tumor DNA (ctDNA)Technology. ARUP Laboratories. Available online at https://www.aruplab.com/files/resources/news/ExpertEdge_Bronner.pdf. Accessed June 2019
Pagana, Kathleen D. & Pagana, Timothy J. (2001). Mosby’s Diagnostic and Laboratory Test Reference 5th Edition: Mosby, Inc., Saint Louis, MO
(© 2004). EGFR by FISH. ARUP’s Guide to Clinical Laboratory Testing [On-line information]. Available online at http://www.aruplab.com/guides/clt/tests/clt_a213.jsp#3635067
Check, W. (2004 January). New school of FISH: solid tumor testing. CAP Cover Story [On-line journal article]. Available online at http://www.cap.org/apps/docs/cap_today/cover_stories/0104NewSchoolOfFISH.html
(2004). Epidermal Growth Factor Receptor Assay, Iressa (Gefitinib) responsiveness in lung cancer, EGFR Gene Analysis. Clinical Molecular Diagnostic Laboratory [On-line information]. Available Online at http://www.cityofhope.org/cmdl/EGFR.asp
(© 2003). Epidermal Growth Factor Receptor (EGFR), Breast Cancer. LabCorp [On-line test information]. Available Online at http://www.labcorp.com/datasets/labcorp/html/chapter/
(2004 April 29). Discovery Promises Better Use of Iressa for Lung Cancer. American Cancer Society, ACS News Center [On-line article]. Available online at http://www.cancer.org/docroot/NWS/content/NWS_1_1x_Discovery_Promises_Better_Use_of_Iressa_for_Lung_Cancer.asp
Ang, K. et. al. (2002 December 15). Impact of Epidermal Growth Factor Receptor Expression on Survival and Pattern of Relapse in Patients with Advanced Head and Neck Carcinoma. Cancer Research 62, 7350-7356 [On-line journal]. Available Online at http://cancerres.aacrjournals.org/cgi/content/full/62/24/7350
(2004 April 29). Presence of Gene Mutation Tightly Linked to Drug Effectiveness in Lung Cancer. National Cancer Institute [On-line news]. Available Online at http://www.cancer.gov/newscenter/pressreleases/IressaMutation
Billingsley, J. (2003 December 6). New Clue to Breast Cancer Mortality, Growth factor identified with poorer outcomes in patients. Henry Ford Health System [On-line news]. Available Online at http://www.henryfordhealth.org/110736.cfm
Langreth, R. (2004 April 29). Gene Predicts Cancer Drug Effectiveness. Forbes.com Pharmaceuticals [On-line article]. Available Online at http://www.forbes.com/2004/04/29/cx_rl_0429cancer_print.html
(2003). Epidermal Growth Factor Receptor Status in Breast Cancer Metastases to the Central Nervous System – Comparison With HER-2/neu Status. CAP [On-line Abstracts From the College of American Pathologists 2003 Annual Meeting (CAP ’03)]. Available Online at http://www.cap.org/apps/docs/archives_pathology_lab_med/this_month.html
Weaver, C. and Maxon, J. (1998- 2004). Targeting Epidermal Growth Factor Receptor Pathways. CancerConsultants.com Current Topics in Oncology [On-line information]. Available online at http://www.411cancer.com/syndication/veContent.jsp?ArticleID=egfr_02&ArticleTypeID=CTON
Kuriyan, J. (2006 June 16). Researchers Learn How Epidermal Growth Factor Receptor Is Activated. Howard Hughes Medical Institute [On-line information]. Available online at http://www.hhmi.org/news/kuriyan20060615.html. Accessed on 7-30-08
American Cancer Society [On-line information]. (2007 May 14, Revised). Detailed Guide: Laryngeal and Hypopharyngeal Cancer. What’s New in Laryngeal and Hypopharyngeal Cancer Research and Treatment? Available online through http://www.cancer.org. Accessed on 7-30-08
Chu, E. et. al. (2007 July 25). Expanding Scientific Evidence for Epidermal Growth Factor Receptor-Directed Therapy in Colorectal Cancer and Squamous Cell Carcinoma of the Head and Neck CME. Medscape Today [On-line information]. Available online at http://www.medscape.com/viewprogram/7463. Accessed on 7-30-08
Dacic, S. et. al. (2006 June 6). Significance of EGFR Protein Expression and Gene Amplification in Non-Small Cell Lung Carcinoma. Medscape from Am J Clin Pathol. 2006;125(6):860-865 [On-line information]. Available online at http://www.medscape.com/viewarticle/532262. Accessed on 7-30-08
Grody, W. (2007 January 30). ASCP 2006: Applications of Molecular Methods in Surgical Pathology CME/CMLE. Medscape [On-line information]. Available online at http://www.medscape.com/viewarticle/551100. Accessed on 7-30-08
Timothy S. Uphoff, PhD, D(ABMG), MLS(ASCP)CM. Section Head Molecular Pathology Laboratory, Marshfield Clinic, Marshfield WI.
Cheng, L. et. al. (2011 May 31). The Landscape of EGFR Pathways and Personalized Management of Non-small-cell Lung Cancer. Medscape Today News from Future Oncology. 2011;7(4):519-541 [On-line information]. Available online at http://www.medscape.com/viewarticle/740715_2. Accessed.December 2013
Grenache, D. et. al. (Updated 2013 November). Lung Cancer. ARUP Consult [On-line information]. Available online at http://www.arupconsult.com/Topics/LungCancer.html?client_ID=LTD#tabs=0. Accessed December 2013
(© 1995-2013). Test ID: FEGFR91903 EGFR Mutation Analysis in NSCLC. Mayo Clinic Mayo Medical Laboratories [On-line information]. Available online at http://www.mayomedicallaboratories.com/test-catalog/Clinical+and+Interpretive/61247. Accessed December 2013
Chen, Y. (Updated 2011 August 24). Lung cancer – non-small cell. MedlinePlus Medical Encyclopedia [On-line information]. Available online at http://www.nlm.nih.gov/medlineplus/ency/article/007194.htm. Accessed December 2013
(Updated May 22, 2013) American Cancer Society. Targeted Therapy. Available online at http://www.cancer.org/cancer/lungcancer-non-smallcell/detailedguide/non-small-cell-lung-cancer-treating-targeted-therapies. Accessed December 2013
Raparia K, et al. Molecular Profiling in Non–Small Cell Lung Cancer: A Step Toward Personalized Medicine. Archives of Pathology & Laboratory Medicine 2013 137:4, 481-491. Available online at http://www.archivesofpathology.org/doi/full/10.5858/arpa.2012-0287-RA. Accessed December 2013
(July 15, 2013) Markman M. Genetics of Non-Small Cell Lung Cancer. Medscape Reference article. Available online at http://emedicine.medscape.com/article/1689988-overview. Accessed December 2013
(Oct 21, 2013) Tan W. Non-small Cell Lung Cancer. Medscape Reference article. Available online at http://emedicine.medscape.com/article/279960-overview. Accessed December 2013
Lindeman N, et al. Molecular testing guideline for selection of lung cancer patients for EGFR and ALK tyrosine kinase inhibitors: guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. J Thorac Oncol. 2013 Jul;8(7):823-59